|
▶ 산성 수용액과 염기성 수용액 자세히 보기 |
앞의
[산성
수용액과 염기성 수용액의 성질]에서는
산성 수용액과 염기 수용액이 보여주는 성질만을 살펴보았습니다. 이
자세히 보기에서는 산성 수용액과 염기성 수용액 안에 존재하는 입자들이
어떻게 다른지 살펴봅니다.
산은 물에 녹아 H+
이온을 내어놓고 염기는 물로부터 H+를
빼앗아 OH-
이온을 만들어내지요. 그렇다면 산 또는 염기를 넣기 전 중성의 물에는
H+
이온도 OH-
이온도 없는 걸까요? 아니랍니다. 아주아주 조금이긴 하지만 H+와
OH-가
모두 있답니다. 어디서 생긴 거냐구요? 바로 물로부터 생긴 거지요.
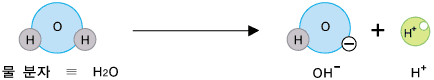
물에 있는 수많은 물 분자 중 아주 일부분이 다음과 같이 나누어 집니다.
|
|
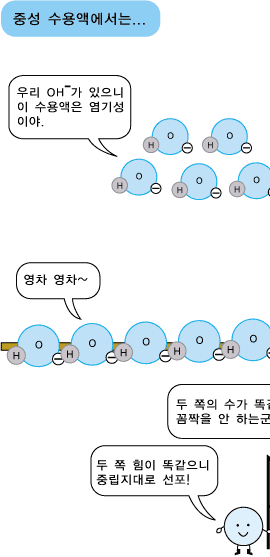
그렇다면 중성의 물에는 H+ 와 OH-가 모두 있는 것인데 왜 중성일까요? 그것은 중성의 물에 있는 H+ 이온의 수와 OH- 이온의 수가 같기 때문입니다.
|
|
|
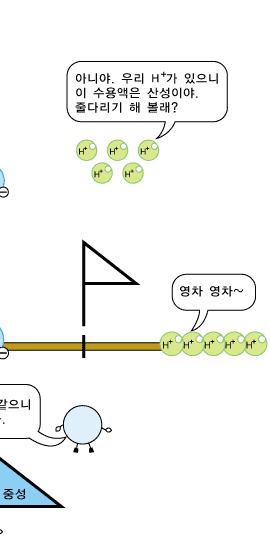
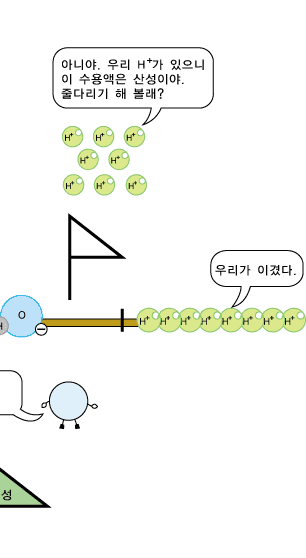
한편 산성 수용액에는 OH- 이온은 전혀 없고 H+ 이온만 있는 걸까요? 그렇지 않답니다. 산성 수용액에도 OH- 이온과 H+ 이온이 모두 있습니다. 그런데 왜 산성이냐구요? 그것은 산성 수용액에는 OH-이온보다 H+ 이온의 수가 더 많아 H+의 성질이 더 두드러지기 때문이랍니다.
|
|
|
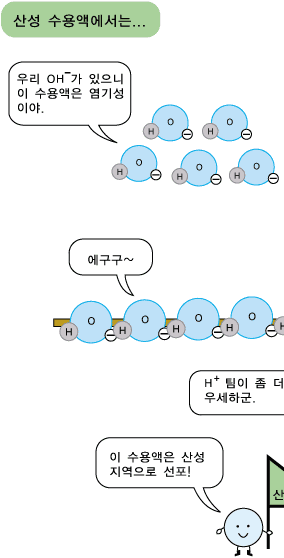
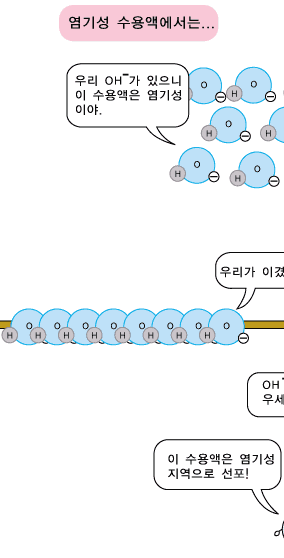
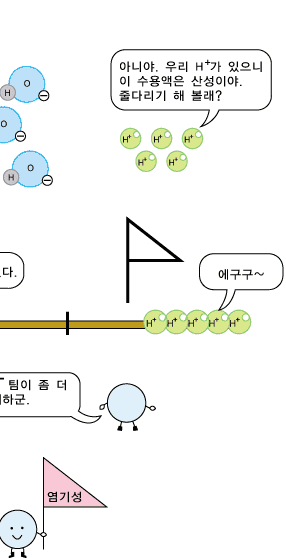
그렇다면 염기성 수용액에서는 어떤 일이 일어나는지 짐작이 가지요? 염기성 수용액에도 OH- 이온과 H+ 이온이 모두 있습니다. 그런데 염기성 수용액에는 OH- 이온의 수가 H+ 이온의 수보다 더 많아 OH-의 성질이 더 두드러지는 것이랍니다.
|
|
|
정리해
볼까요?
모든 수용액에는 H+
이온과 OH-
이온이 항상 같이 있습니다. 두 이온이 같은 수로 있으면 수용액은 중성의
성질을 나타내고, H+
이온의 수가 OH-
이온의 수보다 많으면 용액은 산성의 성질을 나타냅니다. 그리오 OH-
이온의 수가 H+
이온의 수보다 많으면 염기성의 성질을 나타냅니다.
그러니까
용액의 액성은 두 액성을 나타내는 H+와
OH-의
수에 의해 결정되는 것이 아니고 두 이온의 수의 차이에
의해 결정되는 거지요. 우리 주변의 거의 모든 자연 현상은 이렇게 여러
요인의 세기의 차이에
의해 좌우된답니다. 좀 이해가 안 된다 구요? 걱정하지 마세요. 앞으로
자연 현상을 관찰하면서 이러한 예를 많이 만나보게 될 것이고 차차
이해하게 될 거예요.